Các nhà phát triển thuốc điều trị đã tìm kiếm trong thời gian dài các loại thuốc có khả năng tiếp cận thụ thể của tế bào điều hòa các “phản ứng ức chế-stress” trong cơ thể người, nhưng vẫn chưa có loại phân tử nhỏ nào đem lại thành công cho họ. Đến nay, một nhóm nghiên cứu ở Viện Salk đã chứng minh được cách thức của một công cụ mới được sử dụng để lập bản đồ các vùng gắn trên các thụ thể này, điều này cho phép thúc đẩy quá trình xây dựng các liệu pháp điều trị hiệu quả.
Trên tạp chí quốc tế trực tuyến Angewandte Chemie, các nhà nghiên cứu nêu ra phương pháp xác định cách thức các amino acid không tự nhiên (unnatural amino acids, Uaas, amino acid nhân tạo) có thể được sử dụng để lập bản đồ cấu trúc một thụ thể của hormone giải phóng corticotropin (CRF-R1). Họ cũng cho biết cách công cụ mới này hỗ trợ định vị ba vùng trên thụ thể này tạo điều kiện các hormone peptide có thể tác động để kích hoạt hoặc ức chế thụ thể này. Nhiều vùng gắn cho phối tử tự nhiên khác cũng được dự đoán nằm trên thụ thể này.
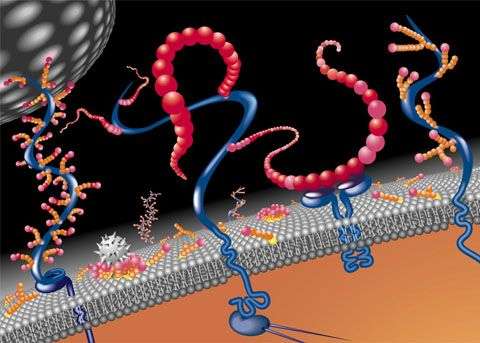
“Thụ thể này rất quan trọng trong việc điều hòa phản ứng stress ở người, chưa ai biết cách thức nó gắn chính xác trên mang tế bào, đây là chìa khóa để hiểu về việc nó thực hiện chức năng như thế nào và có thể được vận hành trong liệu pháp điều trị,” Gs. Irene Coin cho biết. “Chúng tôi đã tạo ra một phương pháp cung cấp một hướng nhìn mới về cách thức các peptide tương tác với thụ thể này.”
Hình minh họa thụ thể trên bề mặt tế bào.
Không chỉ hữu ích cho việc hiểu về chức năng cụ thể của CRF-R1, phương pháp này có thể thích hợp để lập bản đồ các tương tác của những thụ thể gắn cùng G-protein (G-protein-coupled receptors, GPCRs), một họ protein lớn mà trong đó CRF-R1 là một thành viên.
Có hàng trăm GPCRs trong cơ thể người, và chúng là mục tiêu phân tử của hơn 30% dược phẩm ngày nay, Gs. Wang nói. “Kỹ thuật này có tiềm năng lớn hỗ trợ giải đáp các câu hỏi sinh học cơ bản liên quan đến nhiều lớp GPCRs khác nhau, và dẫn lối cho việc phát triển các loại thuốc đặc hiệu cao trong những trường hợp điều trị cụ thể.”
Nghiên cứu này xuất phát từ những khám phá cơ bản của Viện nghiên cứu Salk. Đầu tiên là khám phá vào năm 1981, tạo dòng thụ thể CRF. Thụ thể này gắn trên hormone giải phóng corticotropin, nó điều hòa các đáp ứng ở hệ nội tiết, thần kinh động vật, và miễn dịch trước những stress.
Công cụ mà các nhà nghiên cứu sử dụng bao gồm ba phân tử khác nhau. Một phân tử là RNA (tRNA) có tác dụng vận chuyển các amino acid đến quá trình tổng hợp protein. Phân tử thứ hai là một enzyme synthetase (enzyme tổng hợp cần sự tham gia của ATP) nhận diện được tRNA, và kết hợp nó với phân tử thứ ba-một amino acid nhân tạo. Các amino acid này về mặt hóa học khác với 20 loại amino acid tự nhiên tồn tại trong cơ thể; chúng có thể được chỉnh sửa để có những đặc tính mong muốn, như có khả năng phát quang hoặc tạo phản ứng hóa học khi gặp ánh sáng.
Do biết được trình tự amino acid trên CRF-R1, các nhà nghiên cứu sửa chữa một số vùng cụ thể trên DNA mà họ cho rằng nó có thể nằm gần vùng gắn của phối tử. tRNA được chỉnh sửa và synthetase hoạt động cùng nhau để gắn amino acid nhân tạo này vào các vùng đó. “Chúng tôi có thể kiểm soát được các vị trí mà amino acid đi vào, và chúng tôi đặt chúng vào vị trí mà chúng tôi cho rằng đó là một vùng gắn, dựa trên một số dẫn liệu khác,” Gs. Coin cho biết. “Sau khi gắn các phối tử mang phóng xạ vào các tế bào có các thụ thể đó, các nhà khoa học chiếu ánh sáng, kích hoạt amino acid nhân tạo kìm giữ phối tử nếu phối tử thứ hai tiến lại gần.”
Bằng cách này, các thể đột biến mang một amino acid nhân tạo ở một vị trí khác trên thụ thể có thể được sửa chữa. “Đây là cách để lập bản đồ bề mặt của thụ thể này để quan sát những vị trí nào gần với phối tử,” Gs. Coin nói.
Và các phối tử khác có thể gắn ở vị trí khác trên thụ thể, vì vậy kỹ thuật này có thể được sử dụng để xây dựng một bản đồ đầy đủ về các vị trí gắn đặc hiệu phối tử trên thụ thể, Gs. Wang nói. Với hiểu biết này, các loại dược phẩm được định dạng để gắn đặc hiệu vào vị trí gắn mục tiêu.
Nghiên cứu 12 vị trí khác nhau trên thụ thể, các nhà khoa học tìm thấy ba vùng gắn phối tử tự nhiêu. “Chúng tôi đã công bố phương pháp và bản đồ cơ bản về các vùng gắn. Các phối tử khác lại cho thấy có kiểu gắn kết khác.”
Theo Trần Mạnh Hào (Nguồn Innovations-report)